Doğal olarak oluşan fenoller - Naturally occurring phenols - Wikipedia
İçinde biyokimya, doğal olarak oluşan fenoller ifade eder fenol fonksiyonel grup içinde bulunur doğal ürünler.[1][2][3] Fenolik bileşikler bitkiler ve mikroorganizmalar tarafından üretilir.[4] Organizmalar bazen patojen ve böcek saldırısı, UV radyasyonu ve yaralanma gibi ekolojik baskılara yanıt olarak fenolik bileşikleri sentezler.[5] İnsan diyetlerinde tüketilen gıdalarda ve kullanılan bitkilerde bulundukları için Geleneksel tıp çeşitli kültürlerin insan sağlığı ve hastalıklarındaki rolleri bir araştırma konusudur.[1][5][6][7]:104 Bazı fenoller mikrop öldürücüdür ve dezenfektanların formüle edilmesinde kullanılır.

Sınıflandırma
Çeşitli sınıflandırma şemalar uygulanabilir.[8]:2 Yaygın olarak kullanılan bir şema, karbon sayısına dayanmaktadır ve şu şekilde tasarlanmıştır: Jeffrey Harborne ve 1964'te Simmonds ve 1980'de yayınlandı:[8]:2[9]
| Karbon atomu sayısı | Temel iskelet | Fenolik döngü sayısı | Sınıf | Örnekler |
|---|---|---|---|---|
| 6 | C6 | 1 | Basit fenoller, Benzokuinonlar | Katekol, Hidrokinon, 2,6-Dimetoksibenzokinon |
| 7 | C6-C1 | 1 | Fenolik asitler, Fenolik aldehitler | Gallik, salisilik asitler |
| 8 | C6-C2 | 1 | Asetofenonlar Tirozin türevleri, Fenilasetik asitler | 3-Asetil-6-metoksibenzaldehit, Tyrosol, p-Hidroksifenilasetik asit, Homojentisik asit |
| 9 | C6-C3 | 1 | Hidroksisinamik asitler, Fenilpropenler, Kumarinler, İzokumarinler, Kromonlar | Kafeik, ferulik asitler, Myristicin, Eugenol, Umbelliferone, aesculetin, Bergenon, Eugenin |
| 10 | C6-C4 | 1 | Naftokinonlar | Juglone, Plumbagin |
| 13 | C6-C1-C6 | 2 | Ksantonoidler | Mangiferin |
| 14 | C6-C2-C6 | 2 | Stilbenoidler, Antrakinonlar | Resveratrol, Emodin |
| 15 | C6-C3-C6 | 2 | Kalkonoidler, Flavonoidler, İzoflavonoidler, Neoflavonoidler | Quercetin, cyanidin, Genistein |
| 16 | C6-C4-C6 | 2 | Halojenlenmiş alg fenolik bileşikler | Kaviol A, Colpol |
| 18 | (C6-C3)2 | 2 | Liganlar, Neolignanlar | Pinoresinol, Eusiderin |
| 30 | (C6-C3-C6)2 | 4 | Biflavonoidler | Amentoflavone |
| birçok | (C6-C3)n, (C6)n, (C6-C3-C6)n | n> 12 | Ligninler, Katekol melaninler, Flavolanlar (Yoğun tanenler ), Polifenolik proteinler, Polifenoller | Ahududu ellagitannin, TANIK asit |
Bu Harborne sınıflandırmasında C değildir6-C7-C6 günlük-heptanoidler.
Fenol gruplarının sayısına göre de sınıflandırılabilirler. Bu nedenle çağrılabilirler basit fenoller veya monofenollertek bir fenolik grupla veya di- (iki), üç ve oligofenollersırasıyla iki, üç veya birkaç fenolik grupla.
Çeşitli bir aile doğal fenolleri, flavonoidler birkaç bin bileşiği içeren flavonoller, flavonlar, flavan-3ol (kateşinler), flavanonlar, antosiyanidinler, ve izoflavonoidler.[10]
Fenolik birim, yeni bir polifenol sınıfı oluşturarak dimerleştirilmiş veya daha fazla polimerize edilmiş olarak bulunabilir. Örneğin, elajik asit bir gallik asit dimeridir ve elajitannin sınıfını oluşturur veya kateşin ve bir gallocatechin kırmızı bileşiği oluşturmak için birleşebilir theaflavin, aynı zamanda büyük kahverengi sınıfıyla sonuçlanan bir süreç Thearubigins çayda.
İki farklı kategoriden iki doğal fenol, örneğin bir flavonoid ve bir lignan, aşağıdaki gibi melez bir sınıf oluşturmak için birleşebilir. Flavonolignanlar.
İsimlendirme polimerler:
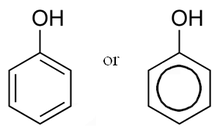
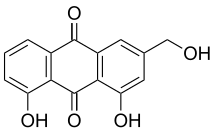
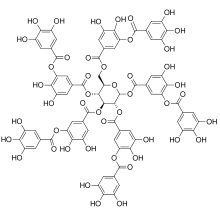
| Ana ünite: |  |  |  |
|---|---|---|---|
| Sınıf / Polimer: | Hidrolize edilebilir tanenler | Flavonoid, Yoğun tanenler |
Hibrit kimyasal sınıflar
Cinsteki bitkiler Humulus ve Kenevir terpenofenolik metabolitler, meroterpenler.[11] Fenolik lipitler fenolik bir kısma bağlı uzun alifatik zincirlerdir.
Kiralite
Birçok doğal fenol, kiral. Bu tür moleküllerin bir örneği kateşin. Cavicularin sıradışı bir makro döngüdür çünkü doğadan izole edilen ilk bileşiktir. Optik Aktivite varlığı nedeniyle düzlemsel kiralite ve eksenel kiralite.
UV görünür soğurma
Doğal fenoller, benzenin optik özelliklerini gösterir, örn. 270 nm'ye yakın absorpsiyon. Göre Woodward kuralları, batokromik kaymalar çoğu kez, bir noktadan kaynaklanan yer değiştirmiş π elektronların varlığını düşündürür. birleşme benzen ile viniller gruplar.[12]
Daha yüksek konjugasyon seviyelerine sahip moleküller bu batokromik kayma fenomenine maruz kaldıkça, görünür spektrumun bir kısmı emilir. Süreçte kalan dalga boyları (genellikle spektrumun kırmızı bölümünde), renk belirli bir maddenin. Sinnamik asitlerle asilasyon antosiyanidinler değiştirilmiş renk tonu (CIE Laboratuvar ton açısı) mor.[13]
İşte bir dizi UV gözle görülür konjugasyon düzeylerine göre soldan sağa sınıflandırılan moleküllerin spektrumları:
 UV görünür spektrumu gallik asit, ile lambda max yaklaşık 270 nm. |  UV görünür spektrumu Ferulik asit 321'de lambda max ve 278 nm'de bir omuz ile. |  UV görünür spektrumu Quercetin 369 nm'de lambda max ile. |  UV görünür spektrumu siyanidin-3-O-glukozit (krizantemin), lambda max 518 nm'de. |
 Kimyasal yapısı gallik asit bir fenolik asit. | 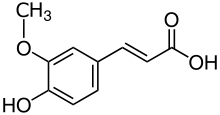 Kimyasal yapısı Ferulik asit bir hidroksisinnamik asit. |  Kimyasal yapısı Quercetin bir flavonol. | 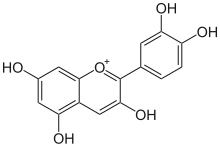 Kimyasal yapısı siyanidin, bir antosiyanidin. |
Kırmızı renginden sorumlu absorbans modeli antosiyaninler yeşilin tamamlayıcısı olabilir klorofil genç gibi fotosentetik olarak aktif dokularda Quercus coccifera yapraklar.[14]
Oksidasyon

Doğal fenoller reaktif karşı türler oksidasyon örneğin gıdalarda bulunan karmaşık fenolik karışımları, otoksidasyon yaşlanma sürecinde. Basit doğal fenoller, B tipi prosiyanidinler şaraplarda[15] veya model çözümlerde.[16][17] Bu, enzimatik olmayan esmerleşme bu sürecin renk değişimi özelliği.[18] Bu fenomen havuç püresi gibi yiyeceklerde görülebilir.[19]
Fenolik bileşiklerin oksidasyonu ile ilişkili esmerleşme, aynı zamanda hücrelerin ölüm nedeni olarak verilmiştir. Calli Içinde oluşturulmuş laboratuvar ortamında kültürler. Bu fenolikler hem eksplant dokularından hem de eksplant sekresyonlarından kaynaklanır.
Fenolik bileşikler
Doğal olarak meydana gelen
| Kanabinoidler | aktif bileşenleri kenevir |
| Kapsaisin | keskin bileşik Şili biberi |
| Carvacrol | bulundu, i.a. kekik; antimikrobiyal ve nöroprotektan[20] |
| Cresol | içinde bulunan kömür katranı ve kreozot |
| Estradiol | estrojen - hormonlar |
| Eugenol | ana bileşeni esans nın-nin karanfil |
| gallik asit | içinde bulunan safra |
| Guaiacol | (2-metoksifenol) - dumanlı lezzet ve bulunur kavrulmuş Kahve, viski, ve Sigara içmek |
| Metil salisilat | uçucu yağın ana bileşeni keklik üzümü |
| Ahududu keton | yoğun bir bileşik Ahududu koku |
| Salisilik asit | öncül bileşik Aspirin (imalatta kimyasal sentez kullanılmaktadır) |
| Serotonin / dopamin / adrenalin / noradrenalin | doğal nörotransmiterler |
| Timol | (2-İzopropil-5-metil fenol) - bulundu Kekik; bir antiseptik kullanılan gargaralar |
| Tirozin | bir amino asit |
| Sesamol | doğal olarak oluşan bir bileşik bulundu Susam taneleri |
Sentetik
| Fenol | olarak kullanılan ana bileşik dezenfektan ve için kimyasal sentez |
| Bisfenol A | ve ketonlardan ve fenol / kresolden üretilen diğer bisfenoller |
| BHT | (butile hidroksitoluen) - yağda çözünür antioksidan ve Gıda katkı maddesi |
| 4-Nonilfenol | bir arıza ürünü deterjanlar ve nonoksinol-9 |
| Ortofenil fenol | a mantar ilacı ağda için kullanılır turunçgiller |
| Pikrik asit | (trinitrofenol) - bir patlayıcı malzeme |
| Fenolftalein | pH göstergesi |
| Ksilenol | antiseptik ve dezenfektanlarda kullanılır |
Biyosentez
Fenolikler, üç farklı biyosentetik yolla oluşturulur: (i) fenil propanoid türevlerini (C6-C3) üreten shikimat / chorizmate veya süksinilbenzoat yolu; (ii) büyük flavonoidler grubu (C6-C3-C6) ve bazı kinonlar dahil olmak üzere yan zincirli uzatılmış fenil propanoidleri üreten asetat / malonat veya poliketid yolu; ve (iii) dehidrojenasyon reaksiyonları ile aromatik terpenoidleri, çoğunlukla monoterpenleri üreten asetat / mevalonat yolu.[21][22] Aromatik amino asit fenilalanin sentezlendi shikimic asit yolu, fenol içeren amino asitler ve fenolik bileşiklerin ortak öncüsüdür.
Bitkilerde fenolik birimler esterlenmiş veya metillenmiş ve gönderildi birleşme bu, doğal fenollerin çoğunlukla glikozit yerine form aglycone form.
Zeytinyağında tirosol Yağ asitleri ile ester oluşturur.[23] Çavdarda alkilresorsinoller fenolik lipitlerdir.
Bazı asetilasyonlar şunları içerir: terpenler sevmek geraniol.[24] Bu moleküller denir meroterpenler (kısmi terpenoid yapıya sahip kimyasal bir bileşik).
Metilasyonlar, bir eter O-metillenmiş polifenolleri oluşturan hidroksil grupları üzerindeki bağ. Durumunda O-metillenmiş flavon mandalina Beş hidroksilin tamamı metillenmiştir ve fenol grubunda serbest hidroksil kalmaz. Metilasyonlar ayrıca doğrudan benzen halkasının bir karbonu üzerinde de meydana gelebilir. poriol, bir C-metillenmiş flavonoid.
Biyolojik bozunma
Beyaz çürük mantar Phanerochaete krisosporium fenolik bileşikleri% 80'e kadar çıkarabilir koklama atık su.[25]
Başvurular
Tanenler bronzlaşma endüstrisinde kullanılmaktadır.
Bazı doğal fenoller şu şekilde kullanılabilir: biyopestisitler. Furanoflavonoidler sevmek Karanjin veya rotenoidler olarak kullanılır akarisit veya böcek ilacı.[26]
Enolojik tanenler şarabın lezzetinde önemli unsurlardır.[27]
Bazı fenoller şu şekilde satılır: diyet takviyeleri. Fenoller ilaç olarak incelenmiştir. Örneğin, Crofelemer (USAN, ticari adı Fulyzaq), anti-HIV ilaçlarıyla ilişkili ishalin tedavisi için geliştirilmekte olan bir ilaçtır. Ek olarak, fenolik bileşikten türevler yapılmıştır, Combretastatin A-4 tedavinin etkinliğini arttırmak için nitrojen veya halojen atomları dahil bir antikanser molekülü.[28]
Endüstriyel işleme ve analiz
Fenol ekstraksiyonu
Fenol ekstraksiyonu endüstriyel ahşap işleme ve kimya endüstrisi için hammadde, bileşik veya katkı maddesi olarak fenolleri hazırlamak için kullanılan bir işleme teknolojisidir.
çıkarma farklı çözücüler kullanılarak gerçekleştirilebilir. Bir risk var polifenol oksidaz (PPO) numunenin fenolik içeriğini düşürür, bu nedenle potasyum gibi PPO inhibitörleri kullanmaya ihtiyaç vardır. ditiyonit (K2S2Ö4) veya sıvı nitrojen kullanarak deney yapmak veya numuneyi birkaç saniye kaynatmak (ağartma ) enzimi inaktive etmek için. Daha ileri fraksiyonlama özü kullanılarak elde edilebilir katı faz ekstraksiyonu sütunlar ve tek tek bileşiklerin izolasyonuna yol açabilir.
Doğal fenollerin biyokütle kalıntısından geri kazanımı, biorefining.[29]
Ayrılık
pKa fenolik bileşiklerin yüzdesi hesaplanabilir saklama süresi içinde sıvı kromatografisi.[30][31]
Analitik Yöntemler
Antioksidan kapasiteyi değerlendirmeye yönelik çalışmalar kullanılabilir elektrokimyasal yöntemler.[32]
Tespit rekombinant ile yapılabilir ışıldayan bakteriyel sensörler.[33]
Profil oluşturma
Fenolik profilleme ile elde edilebilir sıvı kromatografi-kütle spektrometresi (LC / MS).[34]
Niceleme
Fenolik içerik ölçümü için bir yöntem, hacimsel titrasyon. Oksitleyici bir ajan, permanganat, standart bir çözeltinin bilinen konsantrasyonlarını oksitlemek için kullanılır. Standart eğri. Bilinmeyen fenollerin içeriği daha sonra uygun standardın eşdeğerleri olarak ifade edilir.
Toplam fenolik içeriğin miktar tayini için bazı yöntemler, kolorimetrik ölçümler. Toplam fenoller (veya antioksidan etki) kullanılarak ölçülebilir. Folin-Ciocalteu reaksiyonu. Sonuçlar tipik olarak şu şekilde ifade edilir: gallik asit eşdeğerleri (GAE). Demir klorür (FeCl3) Ölçek aynı zamanda kolorimetrik bir tahlildir.
Lamaison ve Carnet, bir numunenin toplam flavonoid içeriğinin belirlenmesi için bir test tasarladı (AlCI3 yöntem). Numunenin ve reaktifin uygun şekilde karıştırılmasından sonra, karışım ortam sıcaklığında 10 dakika inkübe edilir ve solüsyonun absorbansı 440 nm'de okunur. Flavonoid içeriği mg / g kuersetin olarak ifade edilir.[35]
Vasıtasıyla üretilen kantitasyon sonuçları diyot dizisi dedektörü çiftli HPLC genellikle göreli olarak verilir mutlak değerler ticari olarak temin edilebilir bir eksiklik olduğu için standartları her fenolik molekül için. Teknik aynı zamanda birleştirilebilir kütle spektrometrisi (örneğin, HPLC – DAD–ESI / MS) daha hassas molekül için kimlik.
Antioksidan etki değerlendirmesi
- Laboratuvar ortamında ölçümler
Diğer testler, bir fraksiyonun antioksidan kapasitesini ölçer. Bazıları 2,2'-azino-bis (3-etilbenzotiyazolin-6-sülfonik asit) kullanır (ABTS ) fenolikler dahil çoğu antioksidana karşı reaktif olan radikal katyon, tioller ve C vitamini.[36] Bu reaksiyon sırasında mavi ABTS radikal katyonu, renksiz nötr formuna geri dönüştürülür. Reaksiyon, spektrofotometrik olarak izlenebilir. Bu tahlile genellikle Trolox eşdeğer antioksidan kapasitesi (TEAC) analizi. Test edilen çeşitli antioksidanların reaktivitesi aşağıdakilerle karşılaştırılır: Trolox, hangisi bir E vitamini analog.
Standart olarak Trolox kullanan diğer antioksidan kapasite testleri şunları içerir: difenilpikrilhidrazil (DPPH), oksijen radikali emme kapasitesi (ORAC), plazmanın ferrik indirgeme yeteneği (FRAP) analizleri veya bakırla katalize edilen inhibisyon laboratuvar ortamında insan Düşük yoğunluklu lipoprotein oksidasyon.[37]
Bir hücresel antioksidan aktivite (CAA) deneyi de mevcuttur. Diklorofloresin, hücreler içinde sıkışan ve floresana kolayca oksitlenen bir probdur. diklorofloresein (DCF). Yöntem, bileşiklerin DCF oluşumunu önleme yeteneğini ölçer. 2,2'-Azobis (2-amidinopropan) dihidroklorür İnsan hepatokarsinomunda (ABAP) ile oluşturulmuş peroksil radikalleri HepG2 hücreler.[38]
Diğer yöntemler arasında bütillenmiş hidroksitoluen (BHT), bütillenmiş hidroksianisol (BHA), Rancimat yöntemi (yağın bozulma değerlendirmesi).[39]
- İn vivo modeller
Model hayvanın larvaları Galleria mellonella, olarak da adlandırılır balmumu kurtları, tek tek moleküllerin antioksidan etkisini test etmek için kullanılabilir borik asit Gıdada oksidatif strese neden oldu.[40] İçeriği malondialdehit bir oksidatif stres göstergesi ve antioksidan enzimlerin aktiviteleri süperoksit dismutaz, katalaz, glutatyon S-transferaz ve Glutatyon peroksidazı izlenebilir. Bir profesyonelfenoloksidaz böcekten de kurtarılabilir.[41]
Genetik analiz
Fenolik biyosentetik ve metabolik yollar ve enzimler şu şekilde incelenebilir: transgenez genlerin. Arabidopsis üretimi için düzenleyici gen Antosiyanin Pigment 1 (AtPAP1), diğer bitki türlerinde ifade edilebilir.[42]
Doğal olaylar
Fenoller, doğal dünyada, özellikle bitkiler aleminde bulunur.
Prokaryotlarda Oluşumlar
Orobol Içinde bulunabilir Streptomyces neyagawaensis (bir Actinobacterium).[kaynak belirtilmeli ] Fenolik bileşikler şurada bulunabilir: siyanobakteri Arthrospira maximabesin takviyesinde kullanılır, Spirulina.[43] Üç siyanobakteri Microcystis aeruginosa, Cylindrospermopsis raciborskii ve Oscillatoria sp. doğal üretim araştırmalarının konusudur. bütillenmiş hidroksitoluen (BHT),[44] bir antioksidan, gıda katkı maddesi ve endüstriyel kimyasal.
Proteobacterium Pseudomonas fluorescens üretir florosülinol, floroglukinol karboksilik asit ve diasetilfloroglisinol.[45] Proteobakterilerde üretilen fenoliklerin başka bir örneği 3,5-dihidroksi-4-izopropil-trans-stilben bakteriyel bir stilbenoid Photorhabdus bakteriyel simbiyontlar Heterorhabdit nematodlar.
Mantarlarda Oluşumlar
Fenolik asitler mantarda bulunabilir basidiomycetes Türler.[46] Örneğin, protokatekuik asit ve pirokatekol bulunur Agaricus bisporus[47] yanı sıra diğer fenillenmiş maddeler gibi fenilasetik ve fenilpirüvik asitler. Gibi diğer bileşikler Atromentin ve filoforik asit mantarlardan da izole edilebilir. Agarcomycetes sınıf. Orobol, bir izoflavon izole edilebilir Aspergillus niger.
- mayalarda
Aromatik alkoller (örnek: tirosol ) maya tarafından üretilir Candida albicans.[48] Ayrıca şurada bulunurlar bira.[49] Bu moleküller çekirdek algılama için bileşikler Saccharomyces cerevisiae.[50]
- Metabolizma
Aril alkol dehidrojenaz aromatik alkol ve NAD kullanır+ üretmek için aromatik aldehit, NADH ve H+.
Aril alkol dehidrojenaz (NADP +) aromatik alkol ve NADP kullanır+ üretmek için aromatik aldehit, NADPH ve H+.
Arildialkilfosfataz (organofosfor hidrolaz, fosfotriesteraz ve paraokson hidrolaz olarak da bilinir) bir aril dialkil fosfat ve H kullanır2O, dialkil fosfat ve bir aril alkol üretmek için.
Liken oluşumları
Gyroforik asit, bir depside, ve orcinol bulunur liken.[51]
Alglerde oluşum
yeşil alg Botryococcus braunii doğal üretim araştırmalarının konusudur. bütillenmiş hidroksitoluen (BHT),[44] bir antioksidan, gıda katkı maddesi ve endüstriyel kimyasal.
Fenolik asitler, örneğin protocatechuic, p-hidroksibenzoik, 2,3-dihidroksibenzoik, klorojenik, vanilyalı, kafeik, p-kumarik ve salisilik asit, tarçın asidi ve hidroksibenzaldehitler, örneğin p-hidroksibenzaldehit, 3,4-dihidroksibenzaldehit, vanilin tatlı su yeşil alglerinin in vitro kültüründen izole edilmiştir. Spongiochloris spongiosa.[52]
Florotanninler, Örneğin eckol, içinde bulunur kahverengi algler. Vidalenolone tropikal bölgelerde bulunabilir kırmızı alg Vidalia sp.[53]
Kara bitkilerinde (embriyofitler) oluşum
Vasküler bitkilerde oluşumlar
Fenolik bileşikler çoğunlukla damarlı Bitkiler (trakeofitler) yani Lycopodiophyta[54] (likopodlar), Pteridophyta (eğrelti otları ve at kuyrukları), Kapalı tohumlular (çiçekli bitkiler veya Magnoliophyta) ve Gymnospermler[55] (iğne yapraklılar, sikadlar, Ginkgo ve Gnetales ).[kaynak belirtilmeli ]
Eğrelti otlarında, aşağıdaki gibi bileşikler kaempferol ve Onun glukozit izole edilebilir metanolik yaprak özü Phegopteris connectilis[56] veya kaempferol-3-O-rutinosid acı tada sahip olduğu bilinen bir flavonoid glikozit, rizomlarından izole edilebilir. Selliguea ücreti.[57] Hipogallik asit, kafeik asit, Paeoniflorin ve pikurosit tatlı su eğrelti otundan izole edilebilir Salvinia molesta.[58]
Kozalaklı ağaçlarda (Pinophyta), fenolikler polifenolik olarak depolanır. parankim hücrelerde bol miktarda bulunan bir doku floem tüm iğne yapraklıların.[59]
suda yaşayan bitki Myriophyllum spicatum üretir hikâye, Galya ve pirogallik asitler ve (+) -kateşin.[60]
Monokotiledonlarda Oluşumlar
Alkilresorsinoller tahıllarda bulunabilir.[kaynak belirtilmeli ]
2,4-Bis (4-hidroksibenzil) fenol orkidelerde bulunan fenolik bir bileşiktir Gastrodia elata ve Galeola faberi.[kaynak belirtilmeli ]
Damarsız bitkilerde oluşumlar
Fenolikler ayrıca vasküler olmayan kara bitkilerinde de bulunabilir (Briyofitler ). Dihidrostilbenoidler ve bis (bibenziller) ciğerotlarında bulunabilir (Marchantiophyta ), örneğin, makro çevrimler Cavicularin ve Riccardin C. Rağmen lignin yok yosunlar (Bryophyta) ve Hornworts (Anthocerotophyta), bu iki taksonda bazı fenolikler bulunabilir.[61] Örneğin, rosmarinik asit ve bir rosmarinic asit 3'-O-β-D-glukozit, hornwort'ta bulunabilir. Anthoceros agrestis.[62]
Diğer ökaryotlarda oluşumlar
Böceklerde Oluşumlar
Protein bileşeninin sertleşmesi böcek kütikülü Bir fenolik maddenin oksidasyonu ile üretilen bir ajanın tabaklama etkisine bağlı olduğu gösterilmiştir. sklerotin.[kaynak belirtilmeli ] Hamamböceğinin benzer şekilde sertleşmesinde Ootheca, ilgili fenolik madde 3: 4-dihidroksibenzoik asittir (protokatekuik asit ).[63]
Asetosiringon erkek ayaklı böcek tarafından üretilir (Leptoglossus phyllopus ) ve iletişim sisteminde kullanılır.[64][65][66] Guaiacol bağırsaklarında üretilir Çöl çekirgeleri, Schistocerca gregaria, bitki materyalinin parçalanması ile. Bu işlem bağırsak bakterisi tarafından yapılır. Pantoea aglomeranları.[67] Guaiacol, çekirge kümesine neden olan feromonların ana bileşenlerinden biridir.[68] Orcinol karınca türlerinin "toksik tutkalında" tespit edildi Camponotus saundersi.[kaynak belirtilmeli ] Rhynchophorus ferrugineus (kırmızı palmiye kurdu) kullanın 2-metoksi-4-vinilfenol kimyasal sinyalizasyon için (feromonlar ).[69] Diğer basit ve karmaşık fenoller, tümtoplumsal karıncalarda bulunabilir (örneğin Krematogaster ) zehirin bileşenleri olarak.[70]
Memelilerde Oluşumlar
Dişi fillerde iki bileşik 3-etil fenol ve 2-etil 4,5 dimetilfenol idrar örneklerinde tespit edildi.[71] Temporal bezlerin salgı muayenesi, fenol, m-kresol ve p-kresol (4-metil fenol) sırasında musth erkekte filler.[72][73][74]
p-Cresol ve o-kresol aynı zamanda insanın bileşenleridir ter.[kaynak belirtilmeli ] P-kresol aynı zamanda önemli bir bileşendir. domuz koku.[75]
4-Etilfenol, 1,2-dihidroksibenzen, 3-hidroksiasetofenon, 4-metil-1,2-dihidroksibenzen, 4-metoksiasetofenon, 5-metoksisalisilik asit, salisilaldehit, ve 3-hidroksibenzoik asit bileşenleri Castoreum, olgun Kuzey Amerika kunduzunun teker keselerinden çıkan eksüda (Castor canadensis ) ve Avrupa kunduzu (Castor fiber ), parfümeride kullanılır.[76]
Roller
Bazı doğal fenol vakalarında, bitkisel olarak bulunurlar. yeşillik cesaretini kırmak otçul durumunda olduğu gibi Batı zehirli meşe.[77]
Topraktaki rolü
İçinde topraklar, daha büyük miktarlarda fenolün ayrışmadan açığa çıktığı varsayılmaktadır. bitki çöpü herhangi bir doğal bitki topluluğundaki akıntıdan ziyade.[kaynak belirtilmeli ] Ölü bitki materyalinin ayrışması, karmaşık organik bileşiklerin yavaşça oksitlenmesine neden olur lignin -sevmek humus veya daha basit formlara (şekerler ve amino şekerler, alifatik ve fenolik organik asitler) ayrıştırmak, bunlar daha sonra mikrobiyal biyokütleye (mikrobiyal humus) dönüştürülür veya yeniden düzenlenir ve daha sonra hümik topluluklara oksitlenir (fulvik ve hümik asitler), bağlanan kil mineralleri ve metal hidroksitler.[kaynak belirtilmeli ] Bitkilerin hümik maddeleri kök sistemlerinden alma ve onları metabolize etme yetenekleri konusunda uzun süredir tartışma olmuştur.[kaynak belirtilmeli ] Şimdi humusun bitki fizyolojisinde basit bir besleyici rol yerine hormonal bir rol oynadığı konusunda bir fikir birliği var.[kaynak belirtilmeli ]
Toprakta çözünür fenollerin dört farklı kaderi vardır. Aşağıdakiler tarafından bir karbon kaynağı olarak bozunabilir ve mineralize edilebilirler. heterotrofik mikroorganizmalar; çözülmez ve inatçı hale dönüştürülebilirler hümik polimerizasyon ve yoğunlaşma reaksiyonları ile maddeler (toprak organizmalarının katkısıyla); Adsorbe olabilirler kil mineralleri veya form şelatlar alüminyum veya demir iyonları ile; ya da çözünmüş halde kalabilir, süzülerek süzülerek süzülür ve sonunda ekosistemi bir parçası olarak terk edebilirler. çözünmüş organik karbon (DOC).[4]
Sızıntı gibi katyonların kullanıldığı süreçtir Demir (Fe) ve alüminyum (Al) ve ayrıca organik madde, çöplerden çıkarılır ve aşağıdaki toprağa taşınır. Bu süreç olarak bilinir podzolleşme ve özellikle şunlardan oluşan kuzey ve soğuk ılıman ormanlarda yoğundur. iğne yapraklı Çöpleri fenolik bileşikler açısından zengin çamlar ve fulvik asit.[78]
Hayatta kalma rolü
Fenolik bileşikler, istilacı organizmalara, yani otçullara, nematodlara, fitofajlı böceklere ve mantar ve bakteri patojenlerine karşı koruyucu ajanlar, inhibitörler, doğal hayvan toksikleri ve böcek ilaçları olarak hareket edebilir. Diğer fenolikler tarafından verilen koku ve pigmentasyon, meyveleri dağıtan simbiyotik mikropları, tozlayıcıları ve hayvanları çekebilir.[21]
Yırtıcı hayvanlara karşı savunma
Bitkide uçucu fenolik bileşikler bulunur reçine gibi hayırseverleri çekebilecekleri parazitoitler veya avcılar bitkiye saldıran otçulların.[79]
Yosun türlerinde Alaria marginata fenolikler otoburlara karşı kimyasal savunma görevi görür.[80] Tropikal Sargassum ve Turbinaria genellikle tercihli olarak tüketilen türler otçul balıklar ve ekinoidler nispeten düşük düzeyde fenolik ve tanen vardır.[81] Deniz alelokimyasalları genellikle tropikal bölgelerde ılıman bölgelere göre daha fazla miktar ve çeşitlilikte bulunur. Deniz yosunu fenolikleri, bu biyocoğrafik eğilime açık bir istisna olarak rapor edilmiştir. Kahverengi alg türlerinde yüksek fenolik konsantrasyonlar oluşur ( Dictyotales ve Fucales ) hem ılıman hem de tropikal bölgelerden enlem tek başına bitki fenolik konsantrasyonlarının makul bir öngörücüsü değildir.[82]
Enfeksiyona karşı savunma
İçinde Vitis vinifera üzüm, trans-Resveratrol fungal patojenlerin büyümesine karşı üretilen bir fitoaleksin Botrytis cinerea[83] ve delta-viniferin başka bir asma fitoaleksin aşağıdaki üretildi mantar enfeksiyonu tarafından Plasmopara viticola.[84] Pinosylvin bulaşıcıdır stilbenoid toksin (yani enfeksiyondan önce sentezlenir), aksine fitoaleksinler enfeksiyon sırasında sentezlenen. Mevcut öz odun nın-nin Pinaceae.[85] Ahşabı koruyan bir fungitoksindir. mantar enfeksiyonu.[86]
Sakuranetin bir Flavanone, bir tür flavonoid. Bulunabilir Polymnia fruticosa[87] ve pirinç, olduğu yerde fitoaleksin spor çimlenmesine karşı Pyricularia oryzae.[88] İçinde Sorgum, SbF3'H2 gen, kodlayan bir flavonoid 3'-hidroksilaz, şu şekilde ifade ediliyor gibi görünüyor patojen -özel 3-deoksianthocyanidin fitoaleksinler sentez[89] örneğin SorgumColletotrichum etkileşimler.[90]
6-Metoksimellein bir dihidroizokumarin ve bir fitoaleksin havuç dilimlerinde UV-C,[91] direnç sağlayan Botrytis cinerea[92] ve diğeri mikroorganizmalar.[93]
Danielone bir fitoaleksin bulundu papaya meyve. Bu bileşik, yüksek antifungal aktivite gösterdi. Colletotrichum gloesporioides, papaya'nın patojenik bir mantarı.[94]
Stilbenler şu şekilde üretilmektedir: Okaliptüs sideroxylon patojen saldırıları durumunda. Bu tür bileşikler, aşırı duyarlı yanıt bitkilerin. Bazı ahşaplardaki yüksek seviyelerde fenolikler doğal koruma çürümeye karşı.[95]
Bitkilerde, VirA belirli şekerleri ve fenolik bileşikleri algılayan bir protein histidin kinazdır. Bu bileşikler tipik olarak yaralı bitkilerde bulunur ve sonuç olarak VirA, Agrobacterium tumefaciens enfeksiyon için potansiyel konakçı organizmaları bulmak için.[96]
Allelopatik etkileşimlerde rol
Doğal fenoller dahil olabilir allelopatik etkileşimler, örneğin toprak[97] veya suda. Juglon ceviz ağaçlarının etrafındaki diğer bitki türlerinin büyümesini engelleyen böyle bir molekül örneğidir.[kaynak belirtilmeli ] Sucul vasküler bitki Myriophyllum spicatum üretir hikâye, Galya ve pirogallik asitler ve (+) -kateşin mavi-yeşil alglerin büyümesini engelleyen allelopatik fenolik bileşikler Microcystis aeruginosa.[60]
Fenolikler ve özellikle flavonoidler ve izoflavonoidler dahil olabilir endomikoriza oluşumu.[98]
Asetosiringon en iyi bitki-patojen tanımaya katılımıyla bilinir,[99] özellikle cins içindeki benzersiz, onkojenik bakterileri çeken ve dönüştüren bir sinyal olarak rolü Agrobacterium.[kaynak belirtilmeli ] Üzerindeki virA geni Ti plazmid genomunda Agrobacterium tumefaciens ve Agrobacterium rhizogenes bu toprak bakterileri tarafından, asetosiringon için bir reseptör ve bitki yaralarından çıkan diğer fenolik fitokimyasallar için bir reseptör kodlaması yoluyla bitkileri enfekte etmek için kullanılır.[100] Bu bileşik ayrıca bitkilerde, A. tumefaciens aracılı transformasyon prosedürlerinde daha yüksek transformasyon verimine izin verir ve bu nedenle bitki biyoteknolojisinde önemlidir.[101]
İnsan yemeğindeki içerik
Önemli doğal fenol kaynakları insan beslenmesi Dahil etmek çilek, Çay, bira, zeytin yağı, çikolata veya kakao, Kahve, nar, Patlamış mısır, Yerba maté, meyveler ve meyve bazlı içecekler (elma şarabı, şarap ve sirke ) ve sebzeler. Otlar ve baharat, Fındık (ceviz, fıstık) ve yosun ayrıca bazı doğal fenollerin sağlanması için potansiyel olarak önemlidir.
Doğal fenoller ayrıca yağlı matrislerde de bulunabilir. zeytin yağı.[102] Filtresiz zeytinyağı kompleks bir fenol-protein kompleksi oluşturan daha yüksek seviyelerde fenollere veya polar fenollere sahiptir.
Fenolik bileşikler, içecekler, gibi Erik suyu renk ve duyusal bileşenlerde yardımcı olduğu gösterilmiştir. acılık.[103]
Bazı savunucuları Organik tarım organik olarak büyüdüğünü iddia etmek patates, portakallar, ve yaprak sebzeler daha fazla fenolik bileşik içerir ve bunlar sağlayabilir antioksidan e karşı korunma kalp hastalığı ve kanser.[104] Bununla birlikte, organik gıda ile geleneksel gıda arasındaki önemli farklılıklara dair kanıt, organik gıdanın geleneksel gıdalardan daha güvenli veya daha sağlıklı olduğunu iddia etmek için yetersizdir.[105][106]
İnsan metabolizması
Hayvanlarda ve insanlarda, yutulduktan sonra doğal fenoller ksenobiyotik metabolizma. Sonraki faz II reaksiyonlarında, bu aktive edilmiş metabolitler, aşağıdaki gibi yüklü türlerle konjuge edilir. glutatyon, sülfat, glisin veya Glukuronik asit. Bu reaksiyonlar, geniş bir özgünlük transferaz grubu tarafından katalize edilir. UGT1A6 basit fenoller üzerinde aktif olan bir fenol UDP glukuronosiltransferazı kodlayan bir insan genidir.[107] Gen tarafından kodlanan enzim UGT1A8 dahil olmak üzere birçok substrat ile glukuronidaz aktivitesine sahiptir Kumarinler, antrakinonlar ve flavonlar.[108]
Referanslar
- ^ a b Khoddami, A; et al. (2013). "Bitki fenolik bileşiklerinin analizi için teknikler". Moleküller. 18 (2): 2328–75. CiteSeerX 10.1.1.386.9960. doi:10.3390 / moleküller18022328. PMC 6270361. PMID 23429347.
- ^ Amorati, R; Valgimigli, L. (2012). "Kovalent olmayan etkileşimlerle fenollerin antioksidan aktivitesinin modülasyonu". Org Biomol Kimya. 10 (21): 4147–58. doi:10.1039 / c2ob25174d. PMID 22505046.
- ^ Robbins, Rebecca J (2003). "Gıdalarda Fenolik Asitler: Analitik Metodolojiye Genel Bir Bakış". Tarım ve Gıda Kimyası Dergisi. 51 (10): 2866–2887. doi:10.1021 / jf026182t. PMID 12720366.
- ^ a b Hättenschwiler, Stephan; Vitousek, Peter M. (2000). "Karasal ekosistem besin döngüsünde polifenollerin rolü". Ekoloji ve Evrimdeki Eğilimler. 15 (6): 238–243. doi:10.1016 / S0169-5347 (00) 01861-9. PMID 10802549.
- ^ a b Klepacka, J; et al. (2011). "Bazı Bitki Ürünlerinde Kültivar ve Çeşit Ayırıcı Faktörler Olarak Fenolik Bileşikler". Bitki Gıdaları Hum Nutr. 66 (1): 64–69. doi:10.1007 / s11130-010-0205-1. PMC 3079089. PMID 21243436.
- ^ Mishra, BB; Tiwari, VK. (2011). "Doğal ürünler: gelecekteki ilaç keşfinde gelişen bir rol". Eur J Med Chem. 46 (10): 4769–807. doi:10.1016 / j.ejmech.2011.07.057. PMID 21889825.
- ^ Robert E.C. Wildman, Editör. Nutrasötikler ve Fonksiyonel Gıdalar El Kitabı, İkinci Baskı. CRC Press; 2. baskı, 2006. ISBN 0849364094
- ^ a b Wilfred Vermerris ve Ralph Nicholson. Fenolik Bileşik Biyokimyası Springer, 2008
- ^ Harborne, J.B. (1980). "Bitki fenolikleri". Bell, E. A .; Charlwood, B.V. (editörler). Bitki Fizyolojisi Ansiklopedisi, cilt 8 İkincil Bitki Ürünleri. Berlin Heidelberg New York: Springer-Verlag. s. 329–395.
- ^ Jamison Jennifer R. (2003). Hastalık Yönetiminde Beslenme ve Diyet Takviyeleri Klinik Rehberi. s. 525. ISBN 978-0-443-07193-5.
- ^ Bölüm sekiz: "Şerbetçiotu ve kenevirdeki terpenofenolik metabolitlerin biyosentezi". Jonathan E. Page ve Jana Nagel, Fitokimyadaki Son Gelişmeler, 2006, Cilt 40, s. 179–210, doi:10.1016 / S0079-9920 (06) 80042-0
- ^ Jeandenis, J .; Pezet, R .; Tabacchi, R. (2006). "Sıvı kromatografi - atmosferik basınç fotoiyonizasyon kütle spektrometrisi ile tüylü küfle enfekte asma yapraklarından elde edilen stilbenlerin ve türevlerinin hızlı analizi". Journal of Chromatography A. 1112 (1–2): 263–8. doi:10.1016 / j.chroma.2006.01.060. PMID 16458906.
- ^ Stintzing, F. C .; Stintzing, A. S .; Carle, R .; Frei, B .; Wrolstad, R. E. (2002). "Siyanidin Bazlı Antosiyanin Pigmentlerinin Renk ve Antioksidan Özellikleri". Tarım ve Gıda Kimyası Dergisi. 50 (21): 6172–6181. doi:10.1021 / jf0204811. PMID 12358498.
- ^ Karageorgou, P .; Manetaş, Y. (2006). "Gençken kırmızı olmanın önemi: Antosiyaninler ve genç yaprakların korunması Quercus coccifera böcek otçulluğundan ve aşırı ışıktan ". Ağaç Fizyolojisi. 26 (5): 613–621. doi:10.1093 / treephys / 26.5.613. PMID 16452075.
- ^ "Şarapta B-tipi prosiyanidinlerin ve (+) - kateşin ve (-) - epikateşinin bir otoksidasyon karışımında B-tipi dehidrodikateşinlerin tandem kütle spektrometrisi". Weixing Sun, Miller Jack M., Kütle Spektrometresi Dergisi, 2003, cilt 38, sayı 4, sayfa 438–446, INIST:14708334
- ^ He, F .; Pan, Q. H .; Shi, Y .; Zhang, X. T .; Duan, C.Q. (2009). "HPLC-MS / MS ile model çözümlerde flavan-3-ols otoksidasyon oligomerlerinin belirlenmesi". Kütle Spektrometresi Dergisi. 44 (5): 633–640. Bibcode:2009JMSp ... 44..633H. doi:10.1002 / jms.1536. PMID 19053150.
- ^ Cilliers, J. J. L .; Singleton, V.L. (1989). "Bir kafeik asit model sisteminde enzimik olmayan otoksidatif fenolik esmerleşme reaksiyonları". Tarım ve Gıda Kimyası Dergisi. 37 (4): 890–896. doi:10.1021 / jf00088a013.
- ^ "Şarapta Kafeik Asidin Nonenzimik Otoksidatif Reaksiyonları". Johannes J. L. Cilliers ve Vernon L. Singleton, Am. J. Enol. Vitic., 1990, 41: 1, s. 84–86, (Öz )
- ^ Talcott, S. T .; Howard, L.R. (1999). "Fenolik Otoksidasyon, İşlenmiş Havuç Püresinde Renk Bozulmasından Sorumludur". Tarım ve Gıda Kimyası Dergisi. 47 (5): 2109–2115. doi:10.1021 / jf981134n. PMID 10552504.
- ^ "Bir Gıda Katkı Maddesi olan Carvacrol, Farelerde Fokal Serebral İskemi / Reperfüzyon Yaralanmasında Nöroproteksiyon Sağlar", Yu vd. 2012 [1]
- ^ a b Bhattacharya, A; et al. (2010). "Gözden Geçirme: Agrobacterium ve Rhizobium enfeksiyonu sırasında bitki fenoliklerinin savunma ve iletişimdeki rolleri". Mol Bitki Pathol. 11 (5): 705–19. doi:10.1111 / j.1364-3703.2010.00625.x. PMC 6640454. PMID 20696007.
- ^ Knaggs, Andrew R. (2001). "Şikimat metabolitlerinin biyosentezi (1999)". Doğal Ürün Raporları. 18 (3): 334–55. doi:10.1039 / b001717p. PMID 11476485.
- ^ Lucas, Ricardo; Comelles, Francisco; Alcántara, David; Maldonado, Olivia S .; Curcuroze, Melanie; Parra, Jose L .; Morales, Juan C. (2010). "Lipofilik Antioksidanların Yüzey Aktif Özellikleri Tirosol ve Hidroksitirosol Yağ Asidi Esterleri: Suda Yağ Emülsiyonlarında Antioksidan Aktivitesinin Doğrusal Olmayan Hipotezi için Potansiyel Bir Açıklama". Tarım ve Gıda Kimyası Dergisi. 58 (13): 8021–6. doi:10.1021 / jf1009928. PMID 20524658.
- ^ Šmejkal, Karel; Grycová, Lenka; Marek, Radek; Lemière, Filip; Jankovská, Dagmar; Forejtníková, Hana; Vančo, Ján; Suchý, Václav (2007). "C-Geranyl Compounds from Paulownia tomentosa Meyveler ". Doğal Ürünler Dergisi. 70 (8): 1244–8. doi:10.1021 / np070063w. PMID 17625893.
- ^ Lu Y; Yan L; Wang Y; Zhou S; Fu J; Zhang J (Haziran 2009). "Hareketsizleştirilmiş beyaz çürüklük mantarı Phanerochaete chrysosporium tarafından koklaşan atık sudan fenolik bileşiklerin biyolojik olarak parçalanması". Tehlikeli Maddeler Dergisi. 165 (1–3): 1091–7. doi:10.1016 / j.jhazmat.2008.10.091. PMID 19062164.
- ^ Perumalsamy, Haribalan; Jang, Myung Jin; Kim, Jun-Ran; Kadarkarai, Murugan; Ahn, Young-Joon (2015). "Millettia pinnata tohumunda tespit edilen dört flavonoid ve iki yağ asidinin üç sivrisinek türüne yönelik larvisidal aktivitesi ve olası etki şekli". Parazitler ve Vektörler. 8 (1): 237. doi:10.1186 / s13071-015-0848-8. ISSN 1756-3305. PMC 4410478. PMID 25928224.
- ^ Şarap Endüstrisinde Tannin ile İlgili Yeniliklerin Pazar Potansiyeli, Megan Hill ve Geoff Kaine, Victoria Hükümeti Birincil Endüstriler Departmanı, 2007
- ^ Carr, Miriam; Greene, Lisa M .; Knox, Andrew J.S .; Lloyd, David G .; Zisterer, Daniela M .; Meegan, Mary J. (2010). "Konformasyonel olarak kısıtlanmış β-laktam tipi kombretastatin analoglarının kurşun tanımlaması: Sentez, antiproliferatif aktivite ve tubulin hedefleme etkileri". Avrupa Tıbbi Kimya Dergisi. 45 (12): 5752–5766. doi:10.1016 / j.ejmech.2010.09.033. PMID 20933304.
- ^ Villaverde, J. J .; De Vega, A .; Ligero, P .; Freire, C. S. R .; Neto, C. P .; Silvestre, A.J.D. (2010). "Miscanthus x giganteus Kabuk Organosolv Fraksiyonasyonu: Lipofilik Bileşenlerin Kaderi ve Değerli Fenolik Yan Ürünlerin Oluşumu". Tarım ve Gıda Kimyası Dergisi. 58 (14): 8279–8285. doi:10.1021 / jf101174x. PMID 20593898.
- ^ Hanai, T .; Koizumi, K .; Kinoshita, T .; Arora, R .; Ahmed, F. (1997). "PK'nın tahminia hesaplamalı kimyasal analiz ile fenolik ve nitrojen içeren bileşiklerin değerleri sıvı kromatografi ile ölçülenlere kıyasla ". Journal of Chromatography A. 762 (1–2): 55–61. doi:10.1016 / S0021-9673 (96) 01009-6. PMID 9098965.
- ^ Beltran, J. (2003). "Spektrofotometrik, potansiyometrik ve kromatografik pKa su ve asetonitril-su ortamındaki polifenolik asitlerin değerleri ". Analytica Chimica Açta. 484 (2): 253–264. doi:10.1016 / S0003-2670 (03) 00334-9.
- ^ René, Alice; Abasq, Marie-Laurence; Hauchard, Didier; Hapiot Philippe (2010). "Fenolik Bileşikler Süperoksit İyonuna Nasıl Tepkimeye Girer? Antioksidan Kapasitesini Değerlendirmek İçin Basit Bir Elektrokimyasal Yöntem". Analitik Kimya. 82 (20): 8703–10. doi:10.1021 / ac101854w. PMID 20866027.
- ^ Leedjarv, A .; Ivask, A .; Virta, M .; Kahru, A. (2006). "Rekombinant ışıldayan bakteri sensörleri ile doğal numunelerden biyoyararlanabilen fenollerin analizi". Kemosfer. 64 (11): 1910–9. Bibcode:2006Chmsp..64.1910L. doi:10.1016 / j.chemosphere.2006.01.026. PMID 16581105.
- ^ Stobiecki, M .; Skirycz, A .; Kerhoas, L .; Kachlicki, P .; Muth, D .; Einhorn, J .; Mueller-Roeber, B. (2006). "Fenolik glikozidik konjugatların profilinin çıkarılması Arabidopsis thaliana LC / MS kullanarak ". Metabolomik. 2 (4): 197–219. doi:10.1007 / s11306-006-0031-5. S2CID 39140266.
- ^ "Teneurs en principaux flavonoides des fleurs de Cratageus monogyna Jacq et de Cratageus Laevigata (Poiret D.C.) en Fonction de la vegetation ". J. L. Lamaison ve A. Carnet, Plantes Medicinales Fitoterapi, 1991, XXV, sayfa 12–16
- ^ Walker, Richard B .; Everette, Jace D. (2009). "Çeşitli Antioksidanların ABTS Radikal Katyon ile Karşılaştırmalı Reaksiyon Oranları". Tarım ve Gıda Kimyası Dergisi. 57 (4): 1156–61. doi:10.1021 / jf8026765. PMID 19199590.
- ^ Meyer, Anne S .; Yi, Ock-Sook; Pearson, Debra A .; Waterhouse, Andrew L .; Frankel, Edwin N. (1997). "Üzümlerdeki Fenolik Antioksidanların Bileşimine İlişkin İnsan Düşük Yoğunluklu Lipoprotein Oksidasyonunun İnhibisyonu (Vitis vinifera)". Tarım ve Gıda Kimyası Dergisi. 45 (5): 1638–1643. doi:10.1021 / jf960721a.
- ^ Wolfe, K. L .; Liu, R.H. (2007). "Hücresel Antioksidan Aktivite (CAA) Antioksidanlar, Gıdalar ve Diyet Takviyelerinin Değerlendirilmesi için Deneyi". Tarım ve Gıda Kimyası Dergisi. 55 (22): 8896–8907. doi:10.1021 / jf0715166. PMID 17902627.
- ^ Astrid; von Gadow, Elizabeth Joubert; Hansmann, Chris F. (1997). "Aspalathin'in Antioksidan Aktivitesinin Rooibos Çayı (Aspalathus linearis), a-Tocopherol, BHT ve BHA'nın Diğer Bitki Fenollerininki ile Karşılaştırılması". J. Agric. Gıda Kimyası. 45 (3): 632–638. doi:10.1021 / jf960281n.
- ^ Hyršl, Pavel; Büyükgüzel, Ender; Büyükgüzel, Kemal (2007). "Borik asit kaynaklı oksidatif stresin Galleria mellonella'da antioksidan enzimler ve hayatta kalma üzerindeki etkileri". Böcek Biyokimyası ve Fizyolojisi Arşivleri. 66 (1): 23–31. doi:10.1002 / kemer 20194. PMID 17694562.
- ^ Kopácek, Petr; Weise, Christoph; Götz, Peter (1995). "Galleria mellonella balmumu güvesinden elde edilen profenoloksidaz: proenzimin saflaştırılması ve karakterizasyonu". Böcek Biyokimyası ve Moleküler Biyoloji. 25 (10): 1081–1091. doi:10.1016/0965-1748(95)00040-2. PMID 8580908.
- ^ Li, Xiang; Gao, Ming-Jun; Pan, Hong-Yu; Cui, De-Jun; Gruber, Margaret Y. (2010). "Mor Kanola: Arabidopsis PAP1 İçeriğindeki Antioksidanları ve Fenolikleri Artırır Brassica napus Yapraklar". Tarım ve Gıda Kimyası Dergisi. 58 (3): 1639–45. doi:10.1021 / jf903527y. PMID 20073469.
- ^ Fenolik bileşiklerin üretimi Spirulina maxima mikroalgler ve hepatotoksisite modeline karşı in vitro koruyucu etkileri. Abd El-Baky Hanaa H., El Baz Farouk K. ve El-Baroty Gamal S., Gıda bilimlerindeki gelişmeler, 2009, cilt 31, sayı 1, sayfa 8-16, INIST:21511068
- ^ a b Babu B .; Wu J. T. (Aralık 2008). "Tatlı Su Fitoplanktonuyla Bir Antioksidan Olarak Doğal Butillenmiş Hidroksitoluen Üretimi" (PDF). Journal of Phycology. 44 (6): 1447–1454. doi:10.1111 / j.1529-8817.2008.00596.x. PMID 27039859. S2CID 26084768.
- ^ Achkar, Cihane; Xian, Mo; Zhao, Huimin; Frost, J.W. (2005). "Floroglisinolün Biyosentezi". J. Am. Chem. Soc. 127 (15): 5332–5333. doi:10.1021 / ja042340g. PMID 15826166.
- ^ Barros, Lillian; Dueñas, Montserrat; Ferreira, Isabel C.F.R .; Baptista, Paula; Santos-Buelga, Celestino (2009). "On altı farklı Portekiz yabani mantar türünde HPLC-DAD-ESI / MS ile fenolik asit tayini". Gıda ve Kimyasal Toksikoloji. 47 (6): 1076–9. doi:10.1016 / j.fct.2009.01.039. PMID 19425182.
- ^ Delsignore, A; Romeo, F; Giaccio, M (1997). "Bazidiomisetlerdeki fenolik maddelerin içeriği". Mikolojik Araştırma. 101 (5): 552–6. doi:10.1017 / S0953756296003206.
- ^ Ghosh, Suman; Kebaara, Bessie W .; Atkin, Audrey L .; Nickerson Kenneth W. (2008). "Candida albicans'ta Aromatik Alkol Üretiminin Düzenlenmesi". Uygulamalı ve Çevresel Mikrobiyoloji. 74 (23): 7211–7218. doi:10.1128 / AEM.01614-08. PMC 2592902. PMID 18836025.
- ^ Szlavko, Clara M. (1973). "Trtptophol, tyrosol ve phenylethanol - Biradaki aromatik ve daha yüksek alkoller". Brewing Enstitüsü Dergisi. 79 (4): 283–288. doi:10.1002 / j.2050-0416.1973.tb03541.x.
- ^ Hogan, Deborah A. (2006). "Yetersayı Algılama: Sosyal Bir Durumda Alkoller". Güncel Biyoloji. 16 (12): R457 – R458. doi:10.1016 / j.cub.2006.05.035. PMID 16782000. S2CID 3970864.
- ^ Robiquet (1829). "Essai analytique des lichens de l'orseille". Annales de chimie et de physique. 42: 236–257.
- ^ Onofrejová, L .; Vašíčková, J .; Klejdus, B .; Stratil, P .; Mišurcová, L .; Kráčmar, S .; Kopecký, J .; Vacek, J. (2010). "Alglerde biyoaktif fenoller: Basınçlı sıvı ve katı faz ekstraksiyon tekniklerinin uygulanması". İlaç ve Biyomedikal Analiz Dergisi. 51 (2): 464–470. doi:10.1016 / j.jpba.2009.03.027. PMID 19410410.
- ^ Yoo, H. D .; Ketchum, S. O .; Fransa, D .; Bair, K .; Gerwick, W.H. (2002). "Tropikal Kırmızı AlgaVidaliasp'tan Yeni Bir Fenolik Metabolit, Vidalenolone". Doğal Ürünler Dergisi. 65 (1): 51–53. doi:10.1021 / np010319c. PMID 11809064.
- ^ Pedersen, J. A .; Øllgaard, B. (1982). "Lycopodium cinsindeki fenolik asitler". Biyokimyasal Sistematiği ve Ekoloji. 10: 3–9. doi:10.1016/0305-1978(82)90044-8.
- ^ Carnachan, S. M .; Harris, P.J. (2000). "Ferulic acid is bound to the primary cell walls of all gymnosperm families". Biyokimyasal Sistematiği ve Ekoloji. 28 (9): 865–879. doi:10.1016/S0305-1978(00)00009-0. PMID 10913848.
- ^ Adam, K. P. (1999). "Phenolic constituents of the fern Phegopteris connectilis". Bitki kimyası. 52 (5): 929–934. doi:10.1016/S0031-9422(99)00326-X.
- ^ Flavonoids and a proanthrocyanidin from rhizomes of Selliguea feei. Baek Nam-In, Kennelly E. J., Kardono L. B. S., Tsauri S., Padmawinata K., Soejarto D. D. and Kinghorn A. D., Bitki kimyası, 1994, cilt. 36, hayır. 2, pp. 513–518, INIST:3300075
- ^ Choudhary, M. I .; Naheed, N .; Abbaskhan, A .; Müşerref, S. G .; Siddiqui, H .; Atta-Ur-Rahman (2008). "Tatlı su eğreltiotu Salvinia molesta'nın fenolik ve diğer bileşenleri". Bitki kimyası. 69 (4): 1018–1023. doi:10.1016 / j.phytochem.2007.10.028. PMID 18177906.
- ^ Krokene, P.; Nagy, N. E.; Krekling, T. (2008). "Traumatic Resin Ducts and Polyphenolic Parenchyma Cells in Conifers". Induced Plant Resistance to Herbivory. s. 147. doi:10.1007/978-1-4020-8182-8_7. ISBN 978-1-4020-8181-1.
- ^ a b Nakai, S. (2000). "Myriophyllum spicatum-released allelopathic polyphenols inhibiting growth of blue-green algae Microcystis aeruginosa". Su Araştırması. 34 (11): 3026–3032. doi:10.1016 / S0043-1354 (00) 00039-7.
- ^ Erickson, M.; Miksche, G. E. (1974). "On the occurrence of lignin or polyphenols in some mosses and liverworts". Bitki kimyası. 13 (10): 2295–2299. doi:10.1016/0031-9422(74)85042-9.
- ^ Vogelsang, K .; Schneider, B .; Petersen, M. (2005). "Production of rosmarinic acid and a new rosmarinic acid 3′-O-β-D-glucoside in suspension cultures of the hornwort Anthoceros agrestis Paton". Planta. 223 (2): 369–373. doi:10.1007/s00425-005-0089-8. PMID 16133208. S2CID 29302603.
- ^ Hackman, R. H.; Pryor, M. G.; Todd, A. R. (1948). "Eklembacaklılarda fenolik maddelerin oluşumu". Biyokimyasal Dergi. 43 (3): 474–477. doi:10.1042 / bj0430474. PMC 1274717. PMID 16748434.
- ^ Acetosyringone on www.pherobase.com, the pheromones data base
- ^ Aldrich, J. R .; Blum, M. S.; Duffey, S. S.; Fales, H. M. (1976). "Male specific natural products in the bug, Leptoglossus phyllopus: Chemistry and possible function". Böcek Fizyolojisi Dergisi. 22 (9): 1201–1206. doi:10.1016/0022-1910(76)90094-9.
- ^ Aldrich, J. R .; Blum, M. S.; Fales, H. M. (1979). "Species-specific natural products of adult male leaf-footed bugs (Hemiptera: Heteroptera)". Kimyasal Ekoloji Dergisi. 5: 53–62. doi:10.1007/BF00987687. S2CID 34346907.
- ^ Dillon, R.J.; Vennard, C.T.; Charnley, A.K. (Nisan 2002). "A Note: Gut bacteria produce components of a locust cohesion pheromone". Uygulamalı Mikrobiyoloji Dergisi. 92 (4): 759–763. doi:10.1046/j.1365-2672.2002.01581.x. ISSN 1364-5072. PMID 11966918. S2CID 8561972.
- ^ Dillon, Rod J.; Vennard, Chris T.; Charnley, A. Keith (2000). "Exploitation of gut bacteria in the locust". Doğa. 403 (6772): 851. doi:10.1038/35002669. PMID 10706273. S2CID 5207502.
- ^ Yarı kimyasal - 2-metoksi-4-vinilfenol, Pherobase.com
- ^ Marlier, J.; Quinet, Y.; Debiseau, J. (2004). "Defensive Behaviour and Biological Activities of the Abdominal Secretion in the Ant Crematogaster Scutellaris (Hymenoptera: Myrmicinae)" (PDF). Davranışsal Süreçler. 67 (3): 427–40. doi:10.1016/j.beproc.2004.07.003. PMID 15518992. S2CID 21599793.
- ^ Urinary, temporal gland, and breath odors from Asian elephants of Mudumalai National Park. L. E. L. Rasmussen and V. Krishnamurthy, Gajah, the Journal of the Asian Elephant Specialist Group, January 2001, Number 20, pages 1-8 (makale )
- ^ Rasmussen, L. E. L.; Perrin, T. E. (1999). "Physiological Correlates of Musth". Fizyoloji ve Davranış. 67 (4): 539–49. doi:10.1016/S0031-9384(99)00114-6. PMID 10549891. S2CID 21368454.
- ^ "Musth in elephants". Deepa Ananth, Zoo's print journal, 15(5), pp. 259-262 (makale Arşivlendi 2018-06-04 at the Wayback Makinesi )
- ^ Adams, J .; Garcia, A.; Foote, C. S. (1978). "Some chemical constituents of the secretion from the temporal gland of the African elephant (Loxodonta africana)". Kimyasal Ekoloji Dergisi. 4: 17–25. doi:10.1007/BF00988256. S2CID 45857570.
- ^ "Why study pig odor?".
- ^ Müller-Schwarze, D .; Houlihan, P. W. (1991). "Kunduzdaki tek castoreum bileşenlerinin feromonal aktivitesi, Castor canadensis". Kimyasal Ekoloji Dergisi. 17 (4): 715–34. doi:10.1007 / BF00994195. PMID 24258917. S2CID 29937875.
- ^ C.Michael Hogan (2008) Western poison-oak: Toxicodendron diversilobum, GlobalTwitcher, ed. Nicklas Stromberg "Arşivlenmiş kopya". Arşivlenen orijinal on 2009-07-21. Alındı 2009-07-21.CS1 Maint: başlık olarak arşivlenmiş kopya (bağlantı)
- ^ Biogeochemistry: An Analysis of Global Change. 2. Baskı. William H. Schlesinger, Academic Press, 1997, 108, 135, 152–158, 180–183, 191–194
- ^ Plant Resins: Chemistry, evolution, ecology, and ethnobotany, by Jean Langenheim, Kereste Presi, Portland, Oregon. 2003
- ^ Steinberg, P. D. (1984). "Algal Chemical Defense Against Herbivores: Allocation of Phenolic Compounds in the Kelp Alaria marginata". Bilim. 223 (4634): 405–407. Bibcode:1984Sci...223..405S. doi:10.1126/science.223.4634.405. PMID 17829890. S2CID 36409146.
- ^ Steinberg, P. D. (1986). "Chemical defenses and the susceptibility of tropical marine brown algae to herbivores". Oekoloji. 69 (4): 628–630. Bibcode:1986Oecol..69..628S. doi:10.1007/BF00410374. PMID 28311627. S2CID 19551247.
- ^ Targett, Nancy M.; Coen, Loren D .; Boettcher, Anne A.; Tanner, Christopher E. (1992). "Biogeographic Comparisons of Marine Algal Polyphenolics: Evidence against a Latitudinal Trend". Oekoloji. 89 (4): 464–470. Bibcode:1992Oecol..89..464T. doi:10.1007/BF00317150. JSTOR 4219911. PMID 28311874. S2CID 5655010.
- ^ F. Favaron, M. Lucchetta, S. Odorizzi, A. T. Pais da Cunha and L. Sella (2009). "The role of grape polyphenols on trans-resveratrol activity against Botrytis cinerea and of fungal laccase on the solubility of putative grape PR proteins" (PDF). Bitki Patolojisi Dergisi. 91 (3): 579–588. doi:10.4454/jpp.v91i3.549 (etkin olmayan 2020-11-10). Alındı 2011-01-22.CS1 Maint: birden çok isim: yazarlar listesi (bağlantı) CS1 Maint: DOI Kasım 2020 itibariyle aktif değil (bağlantı)
- ^ Timperio, A. M.; d’Alessandro, A.; Fagioni, M.; Magro, P.; Zolla, L. (2012). "Production of the phytoalexins trans-resveratrol and delta-viniferin in two economy-relevant grape cultivars upon infection with Botrytis cinerea in field conditions". Plant Physiology and Biochemistry. 50 (1): 65–71. doi:10.1016/j.plaphy.2011.07.008. PMID 21821423.
- ^ Hovelstad, H.; Leirset, I.; Oyaas, K.; Fiksdahl, A. (2006). "Screening Analyses of Pinosylvin Stilbenes, Resin Acids and Lignans in Norwegian Conifers". Moleküller. 11 (1): 103–114. doi:10.3390/11010103. PMC 6148674. PMID 17962750.
- ^ Lee, S.K .; Lee, H. J .; Min, H. Y.; Park, E. J .; Lee, K. M.; Ahn, Y. H .; Cho, Y. J .; Pyee, J. H. (2005). "Antibacterial and antifungal activity of pinosylvin, a constituent of pine". Fitoterapia. 76 (2): 258–260. doi:10.1016/j.fitote.2004.12.004. PMID 15752644.
- ^ "Sakuranetin". home.ncifcrf.gov. Arşivlenen orijinal 2018-12-03 tarihinde. Alındı 2018-12-02.
- ^ Sakuranetin, a flavonone phytoalexin from ultraviolet-irradiated rice leaves, Kodama O., Miyakawa J., Akatsuka T. and Kiyosawa S., Bitki kimyası, 1992, volume 31, number 11, pp. 3807–3809, INIST:4682303
- ^ Shih, C. -H.; Chu, I. K.; Yip, W. K.; Lo, C. (2006). "Differential Expression of Two Flavonoid 3'-Hydroxylase cDNAs Involved in Biosynthesis of Anthocyanin Pigments and 3-Deoxyanthocyanidin Phytoalexins in Sorghum". Plant and Cell Physiology. 47 (10): 1412–1419. doi:10.1093/pcp/pcl003. PMID 16943219.
- ^ "Biosynthesis and regulation of 3-deoxyanthocyanidin phytoalexins induced during Sorgum-Colletotrichum interaction: Heterologous expression in maize". Chopra Surinder, Gaffoor Iffa, Ibraheem Farag, Poster at the American Society of Plant Biologists (Öz Arşivlendi 2011-07-25 de Wayback Makinesi )
- ^ Mercier, J.; Arul, J.; Ponnampalam, R.; Boulet, M. (1993). "Induction of 6-Methoxymellein and Resistance to Storage Pathogens in Carrot Slices by UV-C". Fitopatoloji Dergisi. 137: 44–54. doi:10.1111/j.1439-0434.1993.tb01324.x.
- ^ Hoffman, R .; Heale, J. B. (1987). "Cell death, 6-methoxymellein accumulation, and induced resistance to Botrytis cinerea in carrot root slices". Fizyolojik ve Moleküler Bitki Patolojisi. 30: 67–75. doi:10.1016/0885-5765(87)90083-X.
- ^ Kurosaki, F.; Nishi, A. (1983). "Isolation and antimicrobial activity of the phytoalexin 6-methoxymellein from cultured carrot cells". Bitki kimyası. 22 (3): 669–672. doi:10.1016/S0031-9422(00)86959-9.
- ^ Danielone, a phytoalexin from papaya fruit. Echeverri F., Torres F., Quinones W., Cardona G., Archbold R., Roldan J., Brito I., Luis J. G., and Lahlou U. E.-H., Bitki kimyası, 1997, vol. 44, hayır. 2, pp. 255–256, INIST:2558881
- ^ Hart, John H.; Hillis, W. E. (1974). "Inhibition of wood-rotting fungi by stilbenes and other polyphenols in Okaliptüs sideroxylon". Fitopatoloji. 64 (7): 939–48. doi:10.1094/Phyto-64-939.
- ^ Brencic, Anja; Winans, Stephen C. (March 2005). "Detection of and Response to Signals Involved in Host-Microbe Interactions by Plant-Associated Bacteria". Microbiol Mol Biol Rev. 69 (1): 155–194. doi:10.1128/mmbr.69.1.155-194.2005. PMC 1082791. PMID 15755957.
- ^ Blum, Udo; Shafer, Steven R.; Lehman, Mary E. (1999). "Evidence for Inhibitory Allelopathic Interactions Involving Phenolic Acids in Field Soils: Concepts vs. an Experimental Model". Bitki Bilimlerinde Eleştirel İncelemeler. 18 (5): 673–93. doi:10.1080/07352689991309441.
- ^ Morandi, D. (1996). "Occurrence of phytoalexins and phenolic compounds in endomycorrhizal interactions, and their potential role in biological control". Bitki ve Toprak. 185 (2): 241–305. doi:10.1007/BF02257529. S2CID 30091640.
- ^ "Involvement of acetosyringone in plant-pathogen recognition". Baker C. Jacyn, Mock Norton M., Whitaker Bruce D., Roberts Daniel P., Rice Clifford P., Deahl Kenneth L. and Aver'Yanov Andrey A., Biyokimyasal ve Biyofiziksel Araştırma İletişimi, 2005, volume 328, number 1, pp. 130–136, INIST:16656426
- ^ Schrammeijer, B.; Beijersbergen, A.; Idler, K. B.; Melchers, L. S.; Thompson, D. V.; Hooykaas, P. J. (2000). "Agrobacterium tumefaciens octopine Ti plazmid pTi15955'ten vir bölgesinin sekans analizi". Deneysel Botanik Dergisi. 51 (347): 1167–1169. doi:10.1093 / jexbot / 51.347.1167. PMID 10948245.
- ^ Sheikholeslam, S. N.; Weeks, D. P. (1987). "Acetosyringone promotes high efficiency transformation of Arabidopsis thaliana explants by Agrobacterium tumefaciens". Bitki Moleküler Biyolojisi. 8 (4): 291–298. doi:10.1007/BF00021308. PMID 24301191. S2CID 32005770.
- ^ Gutfinger, T. (1981). "Polyphenols in olive oils". Amerikan Petrol Kimyacıları Derneği Dergisi. 58 (11): 966–8. doi:10.1007 / BF02659771. S2CID 85367601.
- ^ Donovan, Jennifer L.; Meyer, Anne S .; Waterhouse, Andrew L. (1998). "Phenolic Composition and Antioxidant Activity of Prunes and Prune Juice (Prunus domestica)". Tarım ve Gıda Kimyası Dergisi. 46 (4): 1247–1252. doi:10.1021/jf970831x.
- ^ Asami, Danny K. "Comparison of the Total Phenolic and Ascorbic Acid Content of Freeze-Dried and Air-Dried Marionberry, Strawberry, and Corn Grown Using Conventional, Organic, and Sustainable Agricultural Practices". Tarım ve Gıda Kimyası Dergisi (American Chemical Society), 51 (5), 1237–1241, 2003. 10.1021/jf020635c S0021-8561(02)00635-0. Retrieved 10-Apr-2006.
- ^ Smith-Spangler, C.; Brandeau, M. L.; Hunter, G. E.; Bavinger, J. C.; Pearson, M .; Eschbach, P. J.; Sundaram, V.; Liu, H .; Schirmer, P.; Stave, C.; Olkin, I.; Bravata, D. M. (September 4, 2012). "Are organic foods safer or healthier than conventional alternatives?: a systematic review". İç Hastalıkları Yıllıkları. 157 (5): 348–366. doi:10.7326/0003-4819-157-5-201209040-00007. PMID 22944875. S2CID 21463708.
- ^ Blair, Robert. (2012). Organic Production and Food Quality: A Down to Earth Analysis. Wiley-Blackwell, Oxford, UK. ISBN 978-0-8138-1217-5
- ^ "Cloning and substrate specificity of a human phenol UDP glucuronosyltransferase expressed in COS-7 cells". David Harding, Sylvie Fournel-Gigleux, Michael R. Jackson and Brian Burchell, Proc. Natl. Acad. Sci. Amerika Birleşik Devletleri, November 1988, Volume 85, pp. 8381–8385, (Öz )
- ^ Ritter J. K.; Chen F.; Sheen Y. Y.; Tran H. M.; Kimura S.; Yeatman M. T.; Owens I. S. (Mar 1992). "Yeni bir kompleks lokus UGT1, insan bilirubin, fenol ve aynı karboksil uçlu diğer UDP-glukuronosiltransferaz izozimlerini kodlar". J Biol Kimya. 267 (5): 3257–61. PMID 1339448.
Kitabın
- Biochemistry of phenolic compounds, by J. B. Harborne, 1964, Academic Press (Google Kitapları )
- Plant phenolics, by Pascal Ribéreau-Gayon, 1972, Oliver and Boyd Editions (Google Kitapları, ISBN 0050025120, ISBN 9780050025123)
- The Biochemistry of plant phenolics, by C. F. van Sumere and P. J. Lea, Phytochemical Society of Europe, 1985, Clarendon Press (Google Kitapları, ISBN 9780198541707)
- Biochemistry of Phenolic Compounds, by Wilfred Vermerris and Ralph Nicholson, 2006, Springer (Google kitabı )
Dış bağlantılar
Veritabanları
- Phenol-Explorer (phenol-explorer.eu ), a database dedicated to phenolics found in food by Augustin Scalbert, INRA Clermont-Ferrand, Unité de Nutrition Humaine (Human food unit)
- Fenoller -de ChEBI (Chemical Entities of Biological Interest)
- ChEMBLdb, a database of bioactive drug-like small molecules by the European Bioinformatics Institute
- Foodb, a database of compounds found in food